No mundo, aproximadamente 463 milhões de pessoas vivem com diabetes dos tipos 1 e 2. São 9 milhões de pacientes que possuem o tipo 1 da doença, sendo cerca de 1,1 milhão de crianças e adolescentes. Os dados são do Ministério da Saúde e da Associação Europeia para Estudo de Diabetes (EASD).
“A diabetes tipo 1 é uma doença autoimune, crônica, que não tem cura, e as pessoas precisam injetar insulina diariamente”, explica Erika Machado, estudante do terceiro ano do PhD em Engenharia de Tecidos da Universidade de Groningen, e Líder Estudar. Atualmente, ela trabalha em uma pesquisa com células tronco, com objetivo de desenvolver um modelo de transplante que permita que portadores de diabetes tipo 1 não precisem mais aplicar insulina diariamente.
Leia também: Líderes Estudar, maior programa de bolsas do Brasil, abre inscrições para a edição de 2022
“Explicando” é a nova coluna do Estudar Fora que apresenta como funciona o dia a dia de estudantes, pesquisadores e cientistas de diversas universidades do mundo que passaram por programas da Fundação Estudar. Aqui, eles contam um pouco sobre o que pesquisam e como é o trabalho de cientistas mundo afora.
A seguir, conheça a pesquisa da líder Estudar Erika Machado, saiba como estão sendo elaboradas as propostas de tratamento da diabetes tipo 1 e como funciona o desenvolvimento de tratamentos para doenças que afetam milhares de pessoas em todo o mundo.
O que é a diabetes
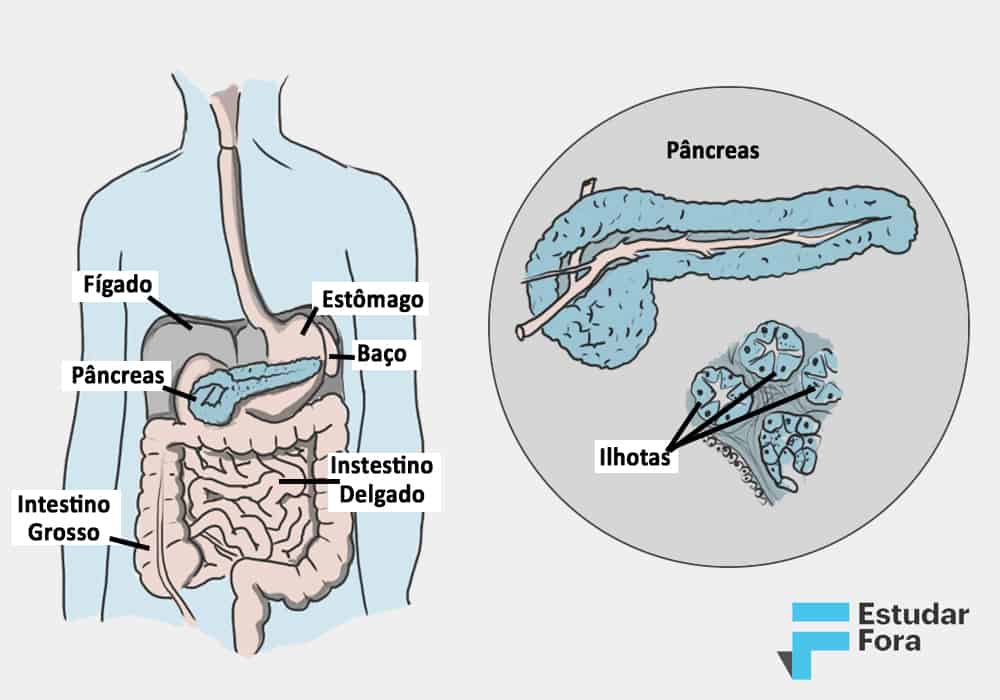
Para o Estudar Fora, a pesquisadora esclarece que as células que produzem insulina, o hormônio que controla a quantidade e absorção de glicose no sangue após a ingestão de alimentos, são parte de uma estrutura no pâncreas chamada Ilhota: “uma ilha de células” que produzem diferentes hormônios “muito importantes para controlar a glicemia, o açúcar do sangue”, explica.
No tipo 1 da doença, as células do organismo que produzem insulina, localizadas no pâncreas, são destruídas pelo próprio sistema autoimune. Neste caso, o paciente fica sem o hormônio no corpo. O tipo 1 “não está relacionado ao estilo de vida”, mas é causado, principalmente, por fatores genéticos. Por ser uma doença crônica, ao contrário do tipo 2, é comum que seja diagnosticada muito cedo em crianças. “Mas também pode surgir depois na vida, com 19, 20 e até 30 anos”, pontua Erika.
No tipo 2, cujo aparecimento geralmente está associado ao estilo de vida da pessoa, “o que acontece é o que a gente chama de resistência à insulina, os hormônios não conseguem regular apropriadamente o açúcar no sangue”.
O tipo 2 da diabetes não é crônico. Hábitos, como sedentarismo, má alimentação, excesso de alimentos com gordura, açúcar e carboidratos e tabagismo fazem com que, com o passar do tempo, as células fiquem exaustas até que, em estágios mais avançados da doença, demandem a injeção de insulina no organismo. Ao contrário do tipo 1, Erika destaca que “no geral, é possível controlar a resistência à insulina com medicamentos”.
Transplante de células para combater a diabetes tipo 1
Por volta de 2001, pesquisadores começaram a estudar formas de transplantar uma ilhota saudável para portadores de diabetes tipo 1. A ideia surgiu a partir da compreensão de que esses pacientes têm essa estrutura atacada pelo sistema autoimune do próprio organismo.
Na primeira tentativa, os pesquisadores tentaram transplantar a ilhota diretamente no pâncreas. Erika conta que os cientistas desenvolveram uma técnica de isolamento da ilhota que utiliza a inserção de enzimas que soltam as células, permitindo que elas sejam filtradas e separadas do órgão original, o pâncreas.
Leia também: Tratar a educação como “bem de consumo” leva a “degradação” do sistema de ensino, afirma ONU
O isolamento da ilhota foi um sucesso, entretanto, ao serem inseridas no pâncreas do paciente, o sistema autoimune destruiu as células transplantadas. Assim, foi necessário encontrar um outro órgão que pudesse receber o transplante. Os pesquisadores descobriram, então,que o fígado seria uma boa alternativa.
Uma segunda tentativa: transplantar as células para o fígado
De acordo com Erika, foi possível inserir as ilhotas, originalmente localizadas no pâncreas, para o fígado, porque são células que precisam de muito sangue para sobreviver. “Elas precisam de um ambiente super vascularizado e o fígado é um dos órgãos mais vascularizados do corpo humano”.
Inicialmente, o transplante foi um sucesso, entretanto, com o passar do tempo, alguns problemas apareceram. Primeiro, os cientistas descobriram que o sistema autoimune também atacava as células no fígado.Neste caso, elas foram rejeitadas por serem transplantadas, ou seja, foram reconhecidas como algo que não pertence originalmente ao corpo.
Um segundo problema encontrado tinha a ver com o tamanho da veia do fígado onde as ilhotas são injetadas. “Elas ficam tão perto umas das outras que acabam entupindo as veias, levando a morte das células”. Depois de 5 anos, os pesquisadores observaram que os pacientes que haviam feito o transplante voltaram a precisar injetar insulina.
A busca por um tratamento definitivo
Por volta de 2005 e 2006, os pesquisadores chegaram à conclusão de que seria necessário encontrar um novo lugar para inserir as ilhotas. “E aí começou essa busca maluca por formas de transplantar ilhotas no corpo humano que possibilitassem maior longevidade para essas células”.
Foi nessa etapa da pesquisa que Erika se juntou a uma das propostas de tratamento da diabetes tipo 1. No hospital da Universidade de Groningen, onde ela estuda, foi desenvolvido um dispositivo feito de um polímero biocompatível, ou seja, que pode ser inserido no corpo humano, cuja estrutura é formada por canais internos onde as ilhotas podem ser inseridas.
Leia também: Vacina AstraZeneca não existiria sem ajuda do Brasil, diz Sue Ann Clemens, cientista de Oxford
Esse dispositivo, que atualmente tem o tamanho de um cartão de microSD, é colocado por baixo da pele através de “um procedimento simples, uma cirurgia minimamente invasiva”, afirma.
Até o momento, o dispositivo precisa ficar na pele do paciente por quatro semanas antes de receber o transplante, para que seja vascularizado e o organismo crie veias, fazendo com que o local passe a ter fluxo sanguíneo. Depois desse período, as ilhotas podem ser transplantadas para o dispositivo, que as “protege do sistema autoimune” do paciente.
Pesquisa com células tronco
Até o momento, os testes feitos em animais com o dispositivo foram um sucesso. Paralelamente, Erika explica que ainda há certos detalhes e problemas para serem resolvidos antes de levar as tentativas para seres humanos.
“Eu pesquiso formas de melhorar e acelerar esse processo de vascularização, para que não precise das quatro semanas antes do transplante, além de pensar em maneiras s de aumentar a barreira para proteger as ilhotas do sistema imune”, conta.
Até o momento, ela está concentrada em uma pesquisa com células tronco retiradas de tecido adiposo. “A gente recebe biópsias de pessoas que fizeram lipoaspiração e eu isolo células tronco dessa gordura, que são muito boas em secretar coisas que ajudam na vascularização”, conclui.
Sobre a líder Erika Machado
Erika Machado entrou para o programa de Líderes Estudar em 2019. Ela é formada em Ciências Biomédicas pela Universidade de São Paulo (USP), com especialização em fisiologia humana. Na graduação, participou do último ano do programa Ciências sem Fronteiras, que a levou para as Universidades de Iowa e Stanford.
Na pós-graduação, os cortes de investimentos em bolsas de pesquisa foram um dos principais motivos que a fizeram considerar realizar um curso fora do país. “Estava procurando alguma oportunidade com bolsa e, no Brasil, eu sabia que não iria conseguir”. Antes de entrar para o doutorado na Universidade de Groningen, ela realizou o mestrado na mesma instituição, onde também participou de um intercâmbio de pesquisa de um ano na Dinamarca.













